臨床試験市場の規模、シェア、トレンド分析レポート:フェーズ別(第I相、第II相、第III相、第IV相)、試験デザイン別(介入試験、観察試験、拡大アクセス試験)、適応症別(自己免疫疾患/炎症、疼痛管理、腫瘍学、中枢神経系疾患、糖尿病、肥満、心血管疾患、その他)、地域別(北米、欧州、アジア太平洋、中東・アフリカ、ラテンアメリカ)の予測、2025年~2033年
臨床試験市場規模
世界の臨床試験市場規模は、2024年には767億米ドルと評価され、2025年の807億1000万米ドルから2033年には1320億5000万米ドルに成長すると予測されており、予測期間(2025年~2033年)中の年平均成長率(CAGR)は6.3%となる見込みです。
臨床試験とは、新薬、治療法、医療機器などの医療介入が人体にどの程度効果があるかを検証するために、綿密に設計された研究です。治療法が広く使用される前に、その安全性と有効性を判断するために不可欠です。
これらの臨床試験は段階的に実施され、それぞれが独自の目的を持っています。
-
フェーズ1:安全性を重視し、少数の被験者で新しい治療法を試験し、副作用や投与量を評価する。
-
フェーズ2:治療効果を評価するとともに、安全性の監視を継続する。
-
フェーズ3:より多くの参加者を対象に、新しい治療法と既存の治療法を比較する。
-
フェーズ4:治療が承認された後に実施され、長期的な効果と安全性を監視する。
臨床試験は厳格なプロトコルに従って実施され、参加者の安全と科学的正確性を確保するために規制機関の監督下に置かれています。これらの研究は、特定の適格基準を満たす個人の自発的な参加に依存しており、参加者は最先端の治療を受ける機会を得ることができます。世界の臨床試験市場の拡大を牽引する主な要因は、特に慢性疾患や複雑な疾患に対する世界的な医療ニーズの急増と、個別化医療および精密医療への注目の高まりです。
臨床試験市場の動向
分散型臨床試験(DCTS)の導入
DCT(分散型臨床試験)とは、遠隔医療、ウェアラブルデバイス、モバイルアプリ、電子同意などの技術を活用し、従来の臨床現場以外で治験を実施するものです。これにより、患者の遠隔参加が可能になり、アクセス性の向上、被験者募集の促進、脱落率の低下、治験期間の短縮につながります。
-
例えば、ファイザーのアトピー性皮膚炎の完全バーチャル治験では、モバイル技術を使用して遠隔患者モニタリングまた、アクセスのしやすさと効率性を向上させるため、DCTのアプローチに沿って、オンライン診療も実施する。
このように、DCTはアクセス性を向上させ、プロセスを効率化し、患者の継続参加率を高めることで、臨床研究をより効率的かつ包括的なものにする。
患者中心の臨床試験デザインへの焦点の移行
患者中心の治験デザインは、参加者の全体的な体験を向上させることに重点を置いており、参加者のニーズ、好み、幸福が治験プロセスの中心となるように配慮しています。このアプローチには、柔軟なプロトコル、個別化されたケア、コミュニケーションを強化し参加者の負担を軽減するためのテクノロジーの活用などが含まれます。
-
例えば、ヤンセン社の「臨床試験における患者の声」プログラムは、患者を試験設計プロセスに積極的に参加させ、患者の意見を収集して試験プロトコルを改善し、患者の参加度を高め、試験が患者のニーズや好みに合致するようにしています。
このように、患者中心の治験デザインは、参加者の体験を向上させ、より良い参加を促し、臨床試験の結果を改善する。
市場概要
| 市場指標 | 詳細とデータ (2025-2034) |
|---|---|
| 2025 市場評価 | USD 94.24 Billion |
| 推定 2026 価値 | USD 100.31 Billion |
| 予測 2034 価値 | USD 165.27 Billion |
| CAGR (2026-2034) | 6.44% |
| 調査期間 | 2022-2034 |
| 主要地域 | 北米 |
| 最も急成長している地域 | アジア太平洋地域 |
| 主要市場プレーヤー | Pharmaceutical Product Development, INC. (Thermo Fisher Scientific, Inc.), ICON plc, Charles River Laboratories International, Inc., IQVIA, SYNEOS HEALTH |

無料サンプルレポートをダウンロード 詳細な洞察を得るために。
臨床試験市場の成長要因
臨床試験数の急増
臨床試験数の増加は市場の主要な推進力であり、多様な治療分野における新たな治療法や治療薬への需要の高まりを反映している。製薬会社やバイオテクノロジー企業は、満たされていない医療ニーズに対応するため研究開発パイプラインを拡大しており、それが臨床試験活動の急増につながっている。
2018年から2025年までの登録臨床試験数は、2019年から2025年(現在まで)にかけて8.18%増加している。
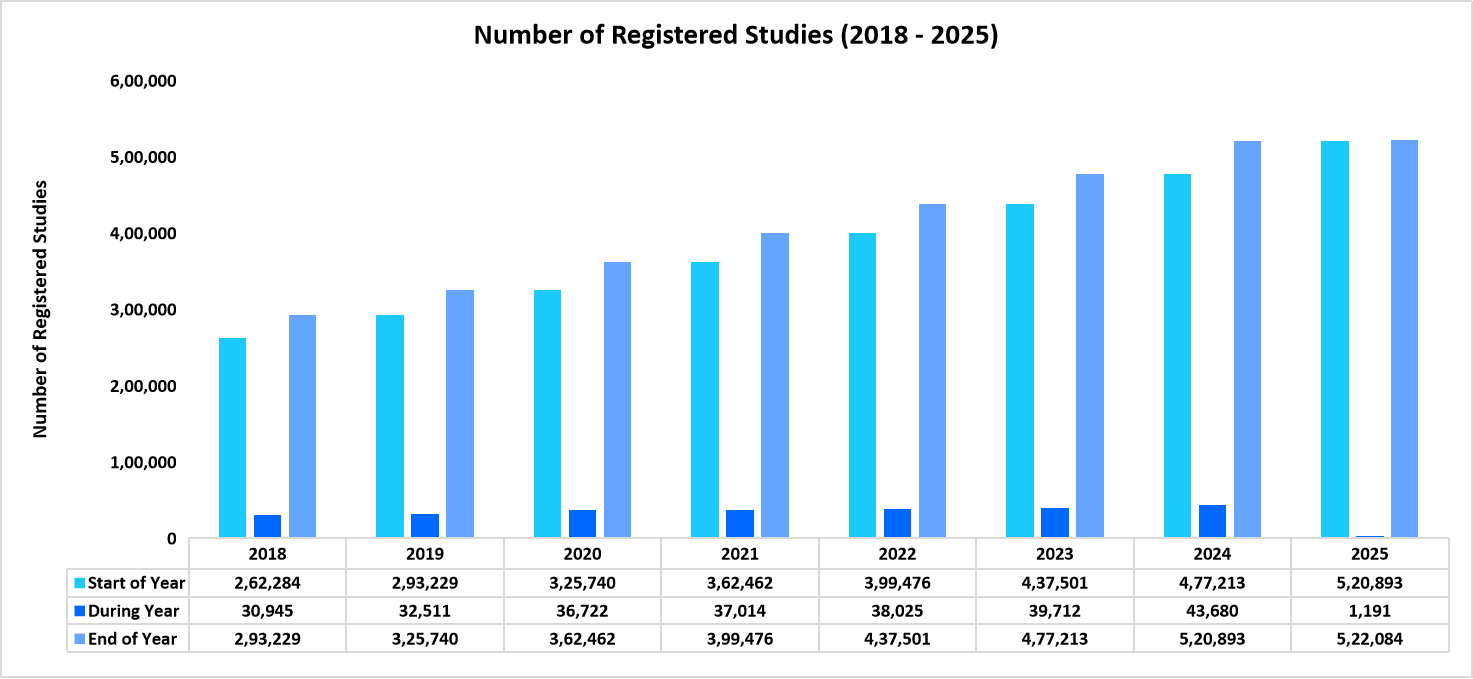
出典:ClinicalTrials.gov
このように、上昇傾向は、新規治療法の必要性、技術の進歩、および様々な治療分野における研究イニシアチブの拡大によって促進される臨床試験への需要の増加を浮き彫りにし、最終的には臨床試験市場の成長に貢献している。
臨床試験のグローバル化
臨床試験のグローバル化は、多様な患者層へのアクセスを可能にし、被験者募集の課題を軽減し、コストを削減することで、市場拡大を促進します。また、試験期間を短縮し、多国間協力を促進することで、規制当局の承認を迅速化し、新薬の市場アクセスを拡大することにつながります。
-
2024年6月にWHOが発表したデータによると、西太平洋地域で登録された臨床試験数(23,250件)は、アフリカ地域(845件)の約14倍でした。この差は主に、中国における臨床試験登録件数の多さに起因しており、これは臨床試験登録を義務付ける中国の学術誌、政府系資金提供機関、大学、病院の増加によるものです。
このように、臨床試験のグローバル化は、患者のアクセス拡大、コスト削減、そして医薬品開発の迅速化に向けた国際協力の促進を通じて、市場の成長を加速させる。
市場抑制要因
患者募集と維持に関する課題
臨床試験業界において、被験者の募集と維持は依然として重要な課題であり、医薬品開発のスピードと成功を著しく阻害する。参加者の不足や高い脱落率は、試験スケジュールを狂わせ、データの完全性を損ない、コストを増加させる。
-
Emmes Company, LLCのホワイトペーパー(2023年9月)によると、臨床試験の85%以上が、試験完了まで十分な参加者を確保できていない。
-
同様に、Md Groupの記事(2020年10月)によると、患者の約30%が、経済的な負担、時間の制約、理解不足や参加意欲の欠如、長距離移動、ストレス、不安、家族の都合などの理由で、治験を完了する前に脱落していると報告されている。
こうした脱落は、遅延、重要なデータの損失、そして代替参加者の募集に伴う経済的負担につながります。MJH Life Sciences(2023年4月)が指摘しているように、脱落した参加者1人を補充するための平均コストは19,533ドルであり、募集プロセスにさらなる負担をかけています。
これらの課題に対処することは、臨床試験の効率性、費用対効果、および成功率を高める上で不可欠です。患者参加戦略の改善、資金援助、および柔軟なスケジュール設定は、これらの問題の軽減に役立ちます。
市場機会
受託研究機関(CRO)の拡大
医薬品開発業務受託機関(CRO)の台頭は、業務の効率化、コスト削減、医薬品開発期間の短縮を通じて、臨床試験業界に大きな変革をもたらす機会となる。CROは、規制遵守、被験者募集、データ管理、治験実施に関する専門知識を提供することで、製薬会社が研究開発に専念することを可能にする。
- サーモフィッシャーサイエンティフィック社(2023年7月)は、欧州のバイオテクノロジー企業が機能サービスプロバイダー(FSP)モデルを採用するCROと提携したと発表しました。この提携により、規制関連業務、メディカルライティング、データ管理といった機能全体にわたるリソースが効率化されました。その結果、提案までの期間が50日以上からわずか36日に短縮され、迅速な事業拡大と効率的なリソース配分が可能になりました。
CRO(医薬品開発業務受託機関)のグローバルなネットワークを活用することで、製薬企業は患者へのアクセスを向上させ、治験の効率を高め、イノベーションを促進することができます。この連携により、新薬の市場投入が加速し、すべての関係者にとってメリットのある状況が生まれます。
地域別分析
北米は、高度な医療インフラ、研究開発への多額の投資、そして大手製薬会社やバイオテクノロジー企業の存在を背景に、臨床試験の世界市場において37.60%という最大の収益シェアを占めています。この地域は、支援的な規制枠組み、多様な患者層、そして試験管理における最先端技術の普及といった恩恵を受けています。これらの要因により、北米は革新的な臨床研究と迅速な医薬品開発のためのグローバルハブとしての地位を確立しています。
米国における臨床試験市場の動向
- 私たち。 -米国は、強固な医療インフラ、多額の研究開発投資、そして数多くの大手製薬会社に支えられ、市場をリードしています。治験管理、規制対応、データ分析を提供するCRO(医薬品開発業務受託機関)が多数集積しているため、米国は国内外の製薬会社を惹きつけています。この確立されたエコシステムは臨床試験プロセスを効率化し、革新的な医薬品開発を可能にし、米国の優位性を維持しています。
アジア太平洋地域の臨床試験市場動向
アジア太平洋地域は、急成長する医療分野、臨床研究への投資増加、そして患者数の増加を背景に、予測期間中に最も高い年平均成長率(CAGR)を示すと予想されています。中国、日本、インドといった国々は、規制環境の改善と費用対効果の高い運営において重要な役割を果たし、世界的な臨床試験の誘致に貢献しています。インフラの強化と革新的な治療法への需要の高まりも、アジア太平洋地域を臨床試験業界における主要な成長牽引力として位置づけています。
- 日本:日本の臨床試験産業は、高齢化、高度な医療インフラ、最先端の医学研究への強い注力に支えられ、急速な成長を遂げています。日本の臨床試験環境は規制がしっかりしており、学術機関や病院の広範なネットワークと相まって、アジアにおける臨床研究のリーダーとなっています。日本はがん、再生医療さらに、個別化された治療は、グローバル市場における同社の役割をさらに強化する。
- 中国:中国は、大規模かつ多様な患者人口、新たな治療法への需要の高まり、そして改善された規制環境を背景に、世界市場における主要プレーヤーとして台頭してきた。医療インフラの急速な拡大に加え、臨床研究を促進するための政府のインセンティブも相まって、中国は特に腫瘍学、心血管疾患、感染症の分野において、臨床試験の魅力的な実施場所となっている。
- インド:インドは、多様な人口構成、高まる医療意識、そして費用対効果の高い治験実施体制を背景に、最も急速に成長している臨床試験市場の一つです。数多くの病院や研究機関を擁する、確立された医療インフラは、臨床試験の拡大を支えています。規制の簡素化に向けた政府の取り組みや、臨床研究への海外投資の増加は、規制プロセスにおける課題はあるものの、インドが新興市場のリーダーとしての地位を確固たるものにしています。
- オーストラリア:オーストラリアの臨床試験業界は、強固な規制枠組み、質の高い医療制度、そして世界レベルの研究機関を特徴としています。多様な患者層と高度な医療技術へのアクセスにより、特に腫瘍学、神経学、免疫学分野における国際的な臨床試験へのオーストラリアの参加は促進されています。オーストラリア政府は研究および臨床試験に対して多大なインセンティブを提供しており、これが市場の成長をさらに後押ししています。
欧州臨床試験市場の動向
- イギリス:英国の強固な医療インフラ、経験豊富な研究機関、そして堅牢な規制枠組みが、同国市場を牽引しています。国民保健サービス(NHS)は多様な患者層を提供し、政府による医療イノベーションへの支援と簡素化された規制が成長を促進しています。学術機関、バイオテクノロジー企業、製薬企業間の連携は、最先端の治療法や療法開発における英国の主要プレーヤーとしての地位を強化しています。
- ドイツ:ドイツは、高度な医療制度、厳格な規制に基づく研究環境、そして強力な製薬産業に支えられ、欧州の臨床試験市場において際立った存在感を放っています。広範な病院と研究センターのネットワークは、腫瘍学、神経学、心臓病学における臨床試験を促進しています。高度なスキルを持つ人材と、イノベーション促進に注力する政府の存在は、臨床研究における主要な拠点としてのドイツの評価をさらに高めています。
- フランス:フランス市場は、腫瘍学、免疫学、希少疾患への注力によって成長を遂げています。充実した医療制度、多様な患者層、そして数多くの臨床試験センターが成長を牽引しています。確立された規制枠組みと多国籍研究イニシアチブへの積極的な参加は、フランスの国際的地位を高めています。さらに、研究開発を支援し、プロセスを効率化する政府の取り組みにより、フランスは臨床研究における主要プレーヤーとなっています。
フェーズインサイト
第III相試験は、大規模な患者参加と、新規治療法の安全性および有効性を確認する上での重要な役割により、世界市場を牽引しています。この段階では、規制当局の承認に必要な包括的なデータが得られるため、医薬品開発の成功に不可欠です。第III相試験に伴う高額な費用とリソースは、治療の信頼性を確保し、公衆衛生上のニーズに効果的に対応する上で、その重要性をさらに際立たせています。
治療領域に関する洞察
がんの罹患率の上昇と革新的な治療法への緊急なニーズを背景に、がん領域は世界の臨床試験市場を牽引しています。がん研究と医薬品開発への多額の投資に加え、標的療法や免疫腫瘍学の進歩が、この分野における臨床試験を加速させています。効果的ながん治療への高い需要は、この領域の優位性をさらに強固なものにし、喫緊のグローバルな健康課題への取り組みにおけるその重要な役割を浮き彫りにしています。
デザインに関する洞察の研究
介入試験分野は、管理された条件下で治療効果と安全性を評価するために広く採用されているため、市場を牽引しています。これらの試験は、規制当局の承認に必要な信頼性の高いデータを生成するために不可欠です。介入試験の構造化されたアプローチは一貫性を確保し、研究者が治療効果をより正確に評価することを可能にします。医薬品開発の基盤として、この分野はイノベーションを推進し、新しい医療介入の信頼性を高めます。
サービスタイプ別の分析
臨床試験データ管理サービスは、臨床データの正確性、完全性、およびセキュリティを確保する上で極めて重要な役割を担っているため、市場を席巻しています。試験がますます複雑化するにつれ、効果的なデータ管理は業務の効率化、規制基準への準拠、そしてリアルタイムの洞察の提供を可能にします。膨大なデータセットを効率的に処理できるこれらのサービスは、意思決定の迅速化と試験結果の向上を支援し、現代の臨床研究において不可欠な存在となっています。
企業別市場シェア
市場の主要企業は、サービス提供の強化、地理的な事業展開の拡大、競争力の強化を目指し、戦略的な提携、買収、パートナーシップを積極的に推進している。企業は、CRO(医薬品開発業務受託機関)、学術機関、バイオテクノロジー企業とのパートナーシップを活用し、業務の効率化と医薬品開発期間の短縮を図っている。
Clinipace(caidya):世界の臨床試験市場における新興プロバイダー
現在Caidyaとしてブランド名を変更したClinipaceは、臨床試験業界における新興リーダーであり、次世代治療法の開発における革新的なアプローチで知られています。同社は特に、がんに対する免疫応答を強化するために新たなチェックポイント経路を標的とする最先端のLAG-3免疫療法で有名です。この画期的な成果により、Caidyaは腫瘍学研究、特に急速に発展している免疫腫瘍学分野において重要な貢献者としての地位を確立しました。
主要および新興プレーヤー一覧 臨床試験市場
- Pharmaceutical Product Development, INC. (Thermo Fisher Scientific, Inc.)
- ICON plc
- Charles River Laboratories International, Inc.
- IQVIA
- SYNEOS HEALTH
- SGS SA
- PAREXEL International Corporation
- Wuxi AppTec, Inc
- Chiltern International Ltd (Laboratory Corporation of America)
- Eli Lilly and Company
- Novo Nordisk A/S
- Pfizer
- Clinipace (Caidya)
- Medpace
- Frontage Labs
最近の動向
- 2025年1月 – シカゴ大学医学部全身性エリテマトーデス、炎症性筋炎、全身性硬化症などの自己免疫疾患に対するCAR T細胞療法の有効性を調査するため、第2相臨床試験を開始した。CAR T細胞療法は、2017年に特定の血液がんに対してFDAの承認を受けたが、現在ではこれらの慢性疾患の治療における可能性が検討されている。
アナリストの意見
アナリストによると、慢性疾患の蔓延、バイオテクノロジーの進歩、個別化医療や革新的な治療法への需要の高まりを背景に、世界市場は力強い成長を遂げています。新興市場における医療インフラの拡大と、治験プロセスを効率化するための規制改革が相まって、市場の発展をさらに加速させています。
さらに、AIやビッグデータ分析といった先進技術の導入は業界を変革し、治験の効率化、コスト削減、そして世界規模での臨床試験の拡張性向上に貢献しています。しかしながら、特に被験者の募集と維持においては課題が残っており、高い脱落率や多様な患者層へのアクセス制限が治験期間の長期化やコスト増加につながっています。
地域ごとの規制の違いも大きな障壁となっており、企業は複雑な法令遵守環境に対応していく必要がある。こうした課題を克服することは、市場の成長と成功を持続させるために不可欠である。
レポート範囲
| レポート指標 | 詳細 |
|---|---|
| 市場規模 2025 | USD 94.24 Billion |
| 市場規模 2026 | USD 100.31 Billion |
| 市場規模 2034 | USD 165.27 Billion |
| CAGR | 6.44% (2026-2034) |
| 推定の基準年 | 2025 |
| 過去データ | 2022-2024 |
| 予測期間 | 2026-2034 |
| レポート範囲 | 収益予測、競争環境、成長要因、環境および規制環境とトレンド |
| 対象セグメント | 段階別, 治療領域別, デザイン研究, サービスの種類別 |
| 対象地域 | 北アメリカ, ヨーロッパ, APAC, 中東諸国とアフリカ, LATAM |
| Countries Covered | アメリカ, カナダ, イギリス, ドイツ, フランス, スペイン, イタリア, ロシア, ノルディック, ベネルクス, ヨーロッパのその他の地域, 中国, 韓国, 日本, インド, オーストラリア, 台湾, 東南アジア, その他のアジア太平洋地域, UAE, トルコ, サウジアラビア, 南アフリカ, エジプト, ナイジェリア, 中東諸国とアフリカの残りの部分, ブラジル, メキシコ, アルゼンチン, チリ, コロンビア, LATAMのその他の地域 |
無料サンプルレポートをダウンロード 詳細な洞察を得るために。
臨床試験市場 セグメント
段階別
- 第I相
- 第II相
- 第III相
- 第IV相
治療領域別
- 感染症
- 疼痛管理
- 腫瘍学
- 中枢神経系の疾患
- 代謝
- 心血管
- その他
デザイン研究
- 介入的
- 観察的
- アクセスの拡大
サービスの種類別
- プロトコル設計
- サイトの識別
- 患者募集
- 検査サービス
- 臨床試験データ管理サービス
- その他
地域別
- 北アメリカ
- ヨーロッパ
- APAC
- 中東諸国とアフリカ
- LATAM
著者の詳細
Debashree B
Healthcare Lead
Debashree Bora is a Healthcare Lead with over 7 years of industry experience, specializing in Healthcare IT. She provides comprehensive market insights on digital health, electronic medical records, telehealth, and healthcare analytics. Debashree’s research supports organizations in adopting technology-driven healthcare solutions, improving patient care, and achieving operational efficiency in a rapidly transforming healthcare ecosystem.










