腫瘍臨床試験市場の規模、シェア、トレンド分析レポート:フェーズ別(第I相、第II相、第III相、第IV相)、タイプ別(乳がん、黒色腫、結腸直腸がん、前立腺がん、肺がん、その他)、研究方法別(介入研究、観察研究、拡大アクセス研究)、地域別(北米、欧州、アジア太平洋、中東・アフリカ、ラテンアメリカ)予測、2026年~2034年
腫瘍臨床試験市場規模・成長分析
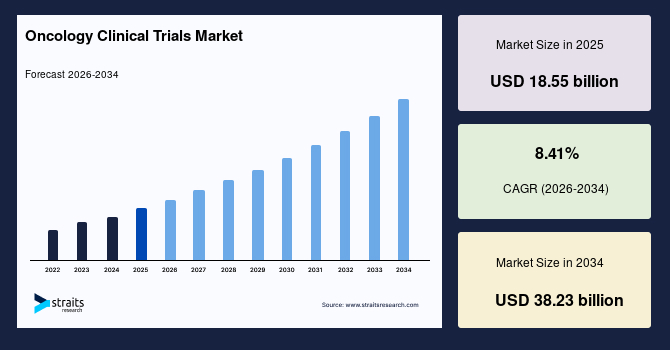
世界のがん臨床試験市場規模は、2025年には185億5000万米ドルと推定され、2034年には382億3000万米ドルに達すると予測されており、予測期間中の年平均成長率(CAGR)は8.41%です。この市場の著しい成長は、免疫腫瘍学分野の進歩と個別化医療への注目の高まりによって促進されており、標的療法や併用療法を評価する臨床試験に対する強い需要を生み出しています。
主要な市場動向と洞察
- 北米は世界市場において圧倒的なシェアを占め、2025年には47.92%のシェアを占める見込みである。
- アジア太平洋地域は、2026年から2034年の予測期間において、年平均成長率(CAGR)9.52%で最も速いペースで成長している。
- フェーズ別に見ると、2025年にはフェーズIセグメントが市場を席巻し、収益シェアは35.26%に達した。
- 種類別に見ると、前立腺がんの分野は、2026年から2034年の予測期間中に9.12%という最も速い年平均成長率(CAGR)を記録すると予想されている。
- 本調査に基づくと、2025年には介入研究分野が市場を席巻し、収益シェアは75.63%になると予測される。
- 米国は世界市場を支配しており、その市場規模は2024年には74億ドル、2025年には79億9000万ドルに達すると予測されている。
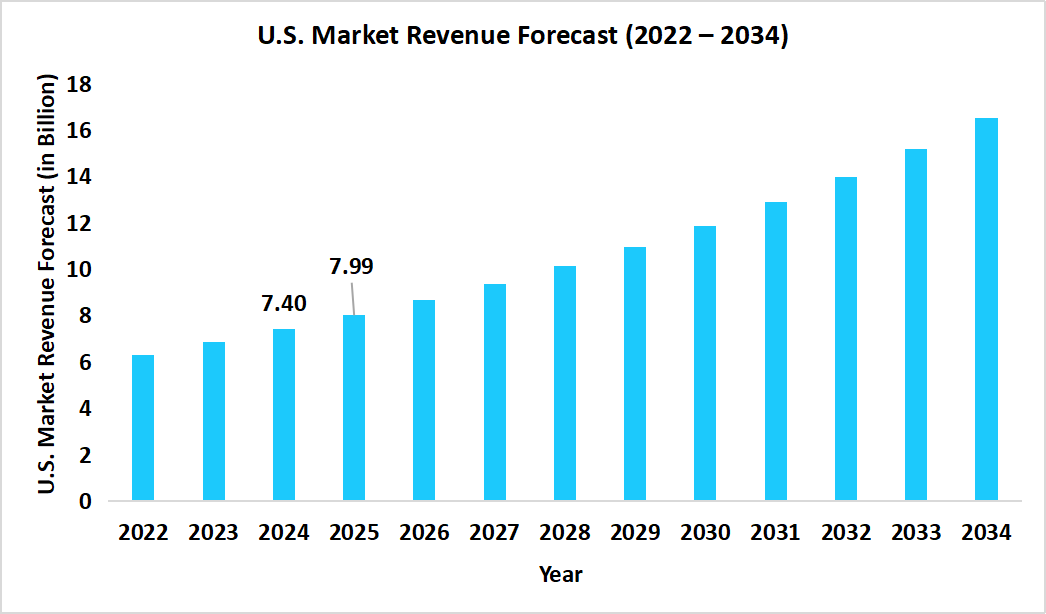
出典:ストレーツ・リサーチ
市場規模と予測
- 2025年の市場規模:185億5000万米ドル
- 2034年の市場規模予測:382億3000万米ドル
- 年平均成長率(2025年~2034年):8.41%
- 支配的な地域:北アメリカ
- 最も成長率の高い地域:アジア太平洋地域
世界の市場は、乳がん、悪性黒色腫、大腸がん、前立腺がん、肺がん、その他の悪性腫瘍など、複数の種類のがんに対する革新的ながん治療薬や治療アプローチの評価に焦点を当てた研究を網羅しています。これらの試験は、第I相、第II相、第III相、第IV相など、さまざまな段階に及び、それぞれが初期の安全性評価から市販後評価まで重要な役割を果たしています。研究デザインに基づき、腫瘍学の臨床試験は、介入試験、観察試験、拡大アクセス試験に分類され、新しい治療法の評価、結果のモニタリング、治験治療の提供を目的としています。市場のエコシステムは、製薬会社やバイオテクノロジー企業、臨床研究機関、学術機関、規制当局などから構成され、これらが連携して臨床開発を推進し、患者募集を効率化し、標的療法、免疫療法、併用療法の進歩を支援し、がん治療成績の向上に貢献しています。
最新の市場動向
細胞・遺伝子治療ががん臨床試験活動の急増を牽引
腫瘍学研究は細胞・遺伝子治療(CGT)へと大きく舵を切り、CAR T細胞療法やTCR細胞療法は、これまで数種類の血液がんにとどまらず、新たな腫瘍タイプへと応用範囲を拡大している。規制当局は新規細胞療法の承認を継続しており、世界中で多数の初期段階の臨床試験が開始されている。FDAの腫瘍学センター・オブ・エクセレンス(OCE)とCBERは、精密診断に関連するものを含む新規細胞療法の承認を報告しており、ClinicalTrials.govでは、世界各地で多数のCAR T/TCR細胞療法の臨床試験が進行中であることが示されている。
この傾向は、第1/2相臨床試験パイプラインの増加を促し、多施設共同治験ネットワークの成長を促進した。より多くの企業が臨床試験プログラムに投資するにつれ、その勢いは腫瘍学臨床試験市場を活性化させ、イノベーションを拡大し、次世代治療法への患者アクセスを向上させた。
放射性医薬品療法が腫瘍学臨床試験の可能性を広げる
がん治療の分野は、放射性医薬品のニッチな用途から、多くの癌種にわたる幅広いパイプラインへと変化しました。かつては前立腺癌や神経内分泌腫瘍に限られていた放射性リガンド療法(RLT)は、現在ではより早期の治療段階、併用療法、そして新たな適応症において試験されています。ノバルティスAGは年次報告書の中で、Pluvictoのグローバル展開とMariana Oncologyの買収により、放射性リガンドのイノベーションに力を入れていると報告しました。
この勢いを受けて、より多くのスポンサーが用量探索試験や多施設共同試験を計画するようになり、試験の範囲と患者グループが拡大した。より多くの製薬会社が放射性医薬品の開発に投資するにつれ、この傾向は世界市場の成長を促進し、イノベーションを推進し、より多くの治療選択肢を開拓した。
市場概要
| 市場指標 | 詳細とデータ (2025-2034) |
|---|---|
| 2025 市場評価 | USD 18.55 billion |
| 推定 2026 価値 | USD 20.04 billion |
| 予測 2034 価値 | USD 38.23 billion |
| CAGR (2026-2034) | 8.41% |
| 調査期間 | 2022-2034 |
| 主要地域 | アジア太平洋 |
| 最も急成長している地域 | 北米 |
| 主要市場プレーヤー | Hoffmann-La Roche Ltd, AstraZeneca, Merck & Co., Inc., Gilead Sciences, Inc , PARAXEL International Corporation |
無料サンプルレポートをダウンロード 詳細な洞察を得るために。
市場の推進要因
国内メーカーによる強力な抗がん剤開発パイプライン
がん臨床試験市場における重要な推進要因は、国内メーカーが開発した強力ながん治療薬開発パイプラインであり、これががん治療における継続的な臨床研究とイノベーションを促進している。
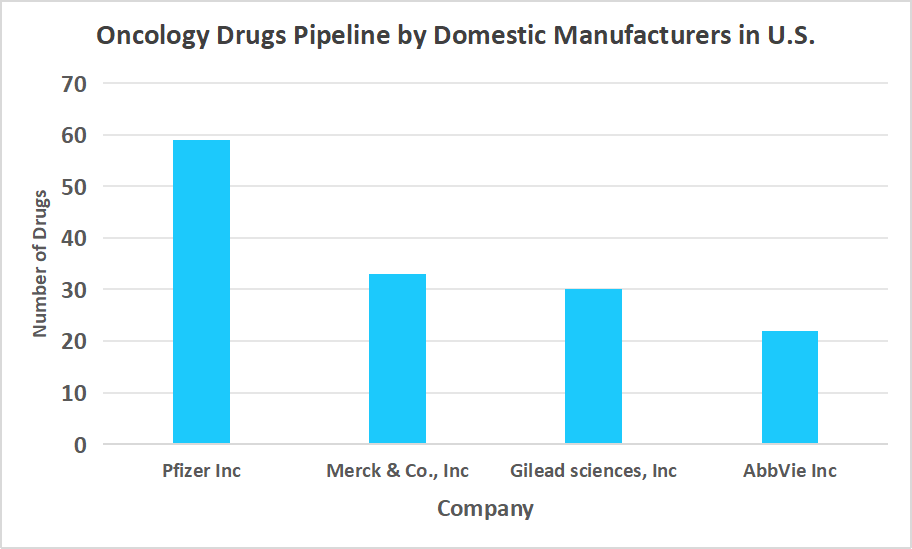
出典:ストレーツ・リサーチ
こうした要因は、市場の成長を支え、患者の治療選択肢を拡大する強力なパイプラインの存在を示していた。
製薬業界への投資が腫瘍市場の拡大を後押し
製薬会社による腫瘍学の研究・製造施設の拡張への投資が市場の成長を牽引しており、その詳細は以下の表に示されている。
表:米国におけるがん研究・製造施設の拡張に向けた製薬会社の投資額
|
日付 |
会社 |
投資額(百万米ドル) |
投資の理由 |
|
2024年2月 |
アストラゼネカ |
300 |
重要な癌臨床試験と将来の商業供給 |
|
2024年7月 |
ベイジーン |
800 |
新規がん治療薬の製造能力と臨床開発能力を拡大する |
|
2024年10月 |
メルクKGaA |
75 |
新規がん治療のための抗体薬物複合体製造の拡大 |
出典:ストレーツ・リサーチ
こうした戦略的投資は、前述の成長要因と相まって、分析期間中の世界市場を牽引している。
市場抑制
がん臨床試験の実施に伴う高コストと複雑さ
がん臨床試験市場における課題の一つは、これらの試験の実施に伴うコストと複雑さの増大である。例えば、2024年2月、米国国立がん研究所(NCI)は、がん臨床試験の開始と運営には多額の費用がかかり、多数の検査、臨床検査、その他のプロトコル要件によって試験期間が長期化することを指摘した。
こうした複雑さは、患者、介護者、研究者の疲労につながり、効果的ながん予防・治療法の提供を遅らせる可能性があった。
市場機会
多様性推進計画ががん臨床試験に新たな道を開く
米国FDAの多様性行動計画は、治験依頼者にとって、より包括的ながん臨床試験を設計する大きな機会となった。これらの計画では、企業は人種、民族、性別、年齢別に明確な被験者登録目標を設定し、その目標をどのように達成するかを説明することが求められた。この変化により、対象となる患者層が拡大し、実社会における臨床試験の関連性が向上した。FDAはFDORAに基づきガイダンス案を発表し、2024年末までに、複数の治験依頼者が多様性に関する期待に応えるため、プロトコルを更新し、新たな地域施設を追加した。
この政策は、治験ネットワークの拡大、被験者募集の障壁の低減、データ一般化可能性の向上をもたらしました。これは腫瘍学分野に新たな機会を生み出しています。臨床試験より幅広い参加とスポンサーの信頼を促進することで市場を活性化させる。
地域分析
北米地域は2025年に47.92%の収益シェアを獲得し、市場を牽引しました。北米市場は、電子カルテ、バイオバンク、集団ゲノムプロジェクトの統合により、治験参加者の募集とモニタリングが効率化されたことで大きく成長しました。米国では、NIHの「All of Us」プログラムのように、2024年までに10万人以上の参加者にゲノム解析結果を返却するなど、治験準備データベースの拡充と個別化治験設計の強化が図られました。こうした統合により、患者識別の障壁が軽減され、治験の多様性が向上し、スポンサーはより迅速かつ正確にがん治験を実施できるようになりました。
米国市場は、臨床試験へのアクセス改善と新たな試験モデルへの資金提供を通じてがん研究の加速を目指す政府の「がんムーンショット計画」により、大幅な市場成長が見込まれています。2024年には、米国国立がん研究所(NCI)が地域密着型の臨床試験ネットワークを拡大し、より多くの地域や医療サービスが行き届いていない地域でがん研究を実施できるようにしました。これにより、試験への参加率が向上し、スポンサー企業は多様な患者環境において実際の治療法を検証する機会を得ることができました。
アジア太平洋市場のインサイト
アジア太平洋地域は、精密医療プログラムに対する政府の強力な支援とゲノムインフラへの多額の投資により、予測期間中に年平均成長率(CAGR)9.52%と最も急速に成長する地域です。中国、日本、韓国などの国々は、がん検査と治験への参加へのアクセスと費用負担を軽減しました。これらの取り組みにより、地域全体でがんの治験が増加しました。
中国市場は、医薬品承認の裏付けとして実世界データ(RWE)の利用を可能にする規制の柔軟性により、著しい市場成長が見込まれている。2024年には、中国国家薬品監督管理局(NMPA)が海南省博鰲市などの試験地域におけるRWEを用いて複数の抗がん剤を承認した。この取り組みは、より多くの企業が中国で抗がん剤の臨床試験を実施するきっかけとなった。
円グラフ:地域別市場シェア、2025年
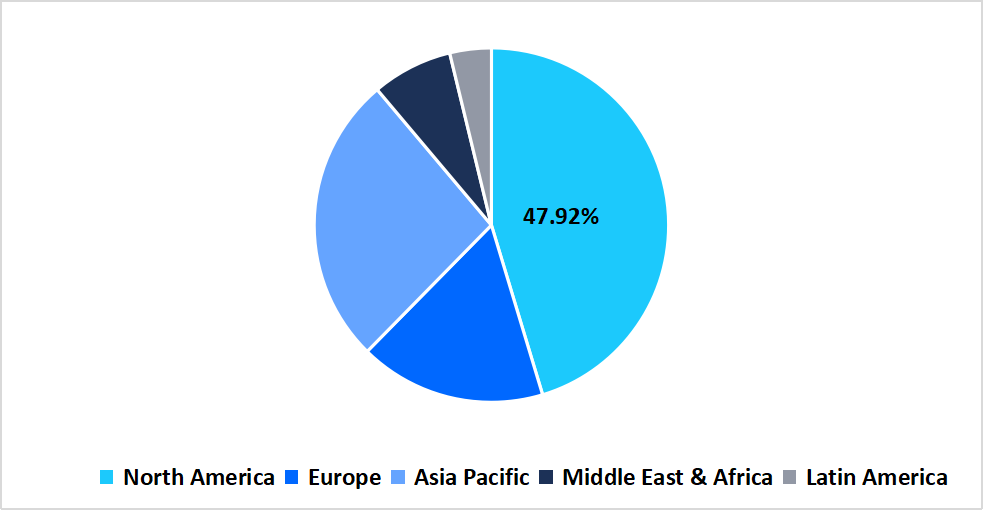
出典:ストレーツ・リサーチ
欧州市場のインサイト
ヨーロッパでは、医療インフラと患者ケア基準の継続的な進歩に牽引され、市場は着実に成長を続けています。ヨーロッパ各国における診断・治療プロトコルの継続的な更新は、革新的な治療法の導入を促進してきました。地域内の多くの癌センターは、新たな癌治療基準に準拠するよう施設をアップグレードしました。こうした改善は、新規抗癌剤や高度な臨床研究への需要を加速させ、ヨーロッパにおける癌臨床試験市場の成長を後押ししています。
スペインでは、あらゆる年齢層におけるがん罹患率の上昇を背景に、がん臨床試験市場が著しく拡大しています。グラフに示すように、がんリスクは年齢とともに顕著に増加し、80~84歳の男性では47.8%、女性では32.7%に達します。この罹患率の上昇は、高度な治療介入と、臨床研究を通じた革新的ながん治療法の継続的な開発が喫緊の課題であることを示しています。
スペインにおける性別・年齢別の癌発症確率(2024年)
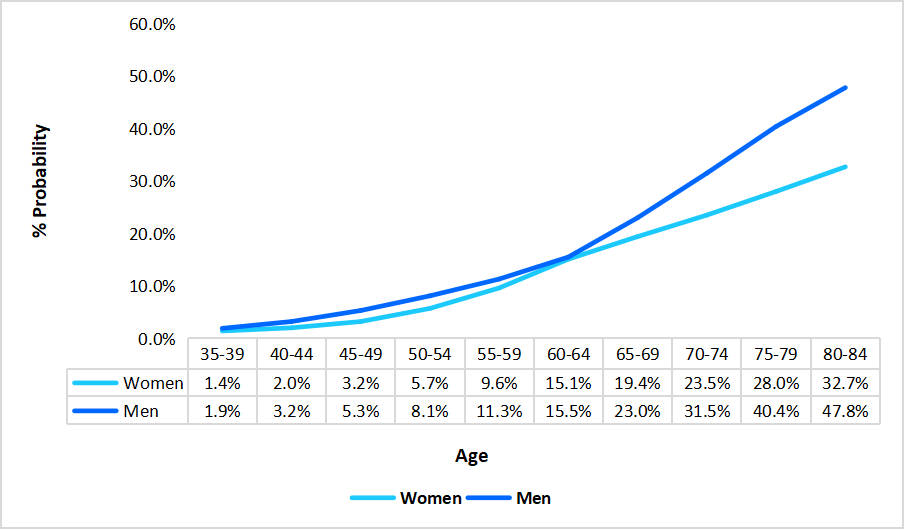
出典:ストレーツ・リサーチ
中東・アフリカ市場のインサイト
中東・アフリカ地域における腫瘍学臨床試験市場は、がん治療インフラの急速な進歩と抗がん剤へのアクセス向上を背景に、着実な成長を遂げている。サウジアラビア、アラブ首長国連邦、南アフリカなどの国々は、がんの診断、治療、研究能力を強化するため、専門のがんセンターに多額の投資を行っている。
南アフリカでは、小児がん治療の向上を目指す取り組みの拡大に伴い、がん臨床試験市場が勢いを増しています。小児がん施設統合地域進化(ProFILE)ツールの導入により、全国規模で小児がん医療サービスの体系的な評価と改善が可能になっています。がん治療の提供体制がより体系化され、公平かつアクセスしやすくなるにつれ、小児がんに対する革新的な抗がん剤や治療法への需要の高まりが、南アフリカ市場の成長に大きく貢献すると予想されます。
ラテンアメリカ市場のインサイト
ラテンアメリカ全域では、全国的ながん検診イニシアチブの普及により、市場は力強い成長を遂げています。ブラジル、メキシコ、アルゼンチンなどの国々は、乳がん、子宮頸がん、大腸がんを対象とした大規模なプログラムを実施し、早期発見と治療成績の向上を図っています。ブラジルの統一医療システム(SUS)を含む政府支援の取り組みにより、予防医療へのアクセスが拡大し、タイムリーな介入が促進され、高度な診断に対する需要が高まっています。抗がん剤そして、この地域における臨床研究。
メキシコは、国内製薬会社からの大規模な投資に支えられ、がん臨床試験の主要拠点として台頭しつつあります。ケネル、ジェンバイオ、ネオルファーマ、ネオルシムの4つのメキシコ製薬会社が7億2200万米ドル以上を投資すると発表したことは、同国のがん臨床試験市場にとって大きなチャンスとなります。がん治療薬の慢性的な不足と革新的な治療法へのアクセス制限が続く中、この投資は、国内の医薬品生産と研究能力の向上を目指す連邦政府の「プラン・メキシコ」構想を支援するものです。これらの投資は、医薬品開発と臨床研究における国内の能力を強化することで、治験開始の加速、患者登録の改善、革新的ながん治療法の利用可能性の向上につながり、国内におけるよりダイナミックで強靭な臨床試験エコシステムの構築を促進します。
フェーズインサイト
第I相セグメントは、初期段階の医薬品開発への注目の高まり、臨床評価に入る新規がん治療薬の増加、およびヒトにおける安全性と投与量の評価の必要性により、2025年には収益シェア35.26%で市場を支配しています。
第III相試験は参加者数が多く費用も高額になるため、予測期間中に年平均成長率(CAGR)9.23%と最も高い成長率を示すと予測されています。これらの試験には、規制当局の承認取得や市販後の義務履行のために実施される長期的な安全性試験も含まれます。
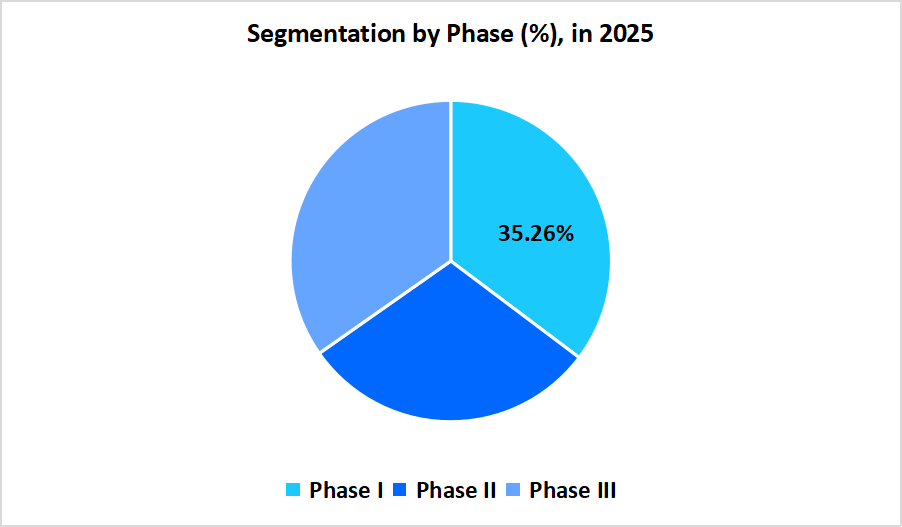
出典:ストレーツ・リサーチ
タイプインサイト
前立腺がん分野は、2026年から2034年にかけて年平均成長率(CAGR)9.12%で成長すると予測されています。この成長は、高齢化に伴う前立腺がんの罹患率の上昇、意識向上と早期発見プログラムの普及、そして革新的な標的療法の開発によるものです。
乳がん分野は、早期発見と個別化治療への強い注力により、市場を牽引し、収益シェアは17.23%を占めた。ホルモン療法、標的療法、免疫療法の継続的な進歩が、広範な研究活動を促進している。さらに、多額の資金提供と啓発活動が、この分野における臨床開発を加速させている。
学習に関する考察
2025年には、介入研究分野が市場を席巻し、収益シェアは75.63%に達した。介入研究は、管理された環境下で実験的治療法を直接検証するため、腫瘍学臨床試験の根幹を成すものであった。安全性と有効性に関する確固たるエビデンスを生み出す能力により、スポンサーや規制当局にとって好ましいアプローチとなり、腫瘍学臨床試験市場の継続的な成長とイノベーションを牽引した。
観察研究は、長期的な患者転帰の追跡調査や市販後調査への重視が高まっていることから、予測期間中に最も高い年平均成長率(CAGR)を記録すると予測されています。これらの研究は、対照試験の枠を超えて、治療効果、安全性、患者の生活の質に関する貴重な知見を提供します。
競争環境
世界の市場は非常に細分化されており、多数の多国籍製薬会社、医薬品開発業務受託機関(CRO)、そして革新的な治療法の開発に積極的に取り組む新興バイオテクノロジー企業が存在する。
OncoNova Therapeutics, Inc.:新興市場のプレーヤー
OncoNova Therapeutics, Inc.は、血液悪性腫瘍および固形腫瘍を標的とした新規低分子治療薬に注力する、グローバル市場における新興企業です。
- 2025年4月、 OncoNova Therapeutics, Inc.は、再発性または難治性の急性骨髄性白血病(AML)患者においてサイクリン依存性キナーゼを阻害するように設計された標的療法である、同社の主要候補薬ONC-123の第II相臨床試験を開始した。
主要および新興プレーヤー一覧 腫瘍臨床試験市場
- Hoffmann-La Roche Ltd
- AstraZeneca
- Merck & Co., Inc.
- Gilead Sciences, Inc
- PARAXEL International Corporation
- ICON plc
- Syneos Health
- Medpace
- Novotech
- Charles River Laboratories
- Laboratory Corporation of America Holdings
- Pfizer Inc.
- Lilly USA, LLC
- Novartis AG
- Bristol-Myers Squibb Company
- AbbVie Inc.
- Amgen Inc.
- Sanofi
- GSK plc.
- Bayer AG
- Others
戦略的イニシアチブ
- 2024年7月:サーモフィッシャーサイエンティフィック社は、米国国立がん研究所と提携し、骨髄腫に対する精密医療を包括的に検証する臨床試験「myeloMATCH」を実施した。
- 2024年3月:バイエルAGとサーモフィッシャーサイエンティフィック社は、次世代シーケンシング(NGS)に基づくコンパニオン診断アッセイの開発で提携した。
- 2024年1月:ペレクセルと日本癌研究振興協会は、日本におけるがん臨床試験へのアクセスを加速させるために協力した。
レポート範囲
| レポート指標 | 詳細 |
|---|---|
| 市場規模 2025 | USD 18.55 billion |
| 市場規模 2026 | USD 20.04 billion |
| 市場規模 2034 | USD 38.23 billion |
| CAGR | 8.41% (2026-2034) |
| 推定の基準年 | 2025 |
| 過去データ | 2022-2024 |
| 予測期間 | 2026-2034 |
| レポート範囲 | 収益予測、競争環境、成長要因、環境および規制環境とトレンド |
| 対象セグメント | 段階別, 種類別, 研究による |
| 対象地域 | 北アメリカ, ヨーロッパ, APAC, 中東諸国とアフリカ, LATAM |
| Countries Covered | アメリカ, カナダ, イギリス, ドイツ, フランス, スペイン, イタリア, ロシア, ノルディック, ベネルクス, ヨーロッパのその他の地域, 中国, 韓国, 日本, インド, オーストラリア, 台湾, 東南アジア, その他のアジア太平洋地域, UAE, トルコ, サウジアラビア, 南アフリカ, エジプト, ナイジェリア, 中東諸国とアフリカの残りの部分, ブラジル, メキシコ, アルゼンチン, チリ, コロンビア, LATAMのその他の地域 |
無料サンプルレポートをダウンロード 詳細な洞察を得るために。
腫瘍臨床試験市場 セグメント
段階別
- 第I相
- 第II相
- 第III相
- 第IV相
種類別
- 乳癌
- メラノーマがん
- 大腸がん
- 前立腺がん
- 肺癌
- その他
研究による
- 介入研究
- 観察研究
- 拡大アクセス研究
地域別
- 北アメリカ
- ヨーロッパ
- APAC
- 中東諸国とアフリカ
- LATAM
著者の詳細
Debashree B
Healthcare Lead
Debashree Bora is a Healthcare Lead with over 7 years of industry experience, specializing in Healthcare IT. She provides comprehensive market insights on digital health, electronic medical records, telehealth, and healthcare analytics. Debashree’s research supports organizations in adopting technology-driven healthcare solutions, improving patient care, and achieving operational efficiency in a rapidly transforming healthcare ecosystem.










