バイオシミラーモノクローナル抗体市場規模
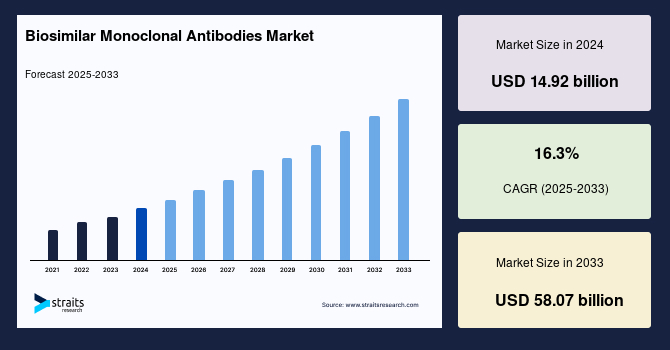
世界のバイオシミラーモノクローナル抗体市場規模は、2024年に149.2億米ドルと評価され、2025年の173.5億米ドルから2033年には580.7億米ドルに達すると予測されています。予測期間(2025~2033年)中、年平均成長率(CAGR)16.3%で成長します。
バイオシミラーモノクローナル抗体(mAb)は、既に承認されているリファレンスモノクローナル抗体と高い類似性を持つように設計された生物学的医薬品であり、安全性、純度、有効性において臨床的に意味のある差異はありません。生細胞を用いて製造されるこれらの抗体は、がん、自己免疫疾患、炎症性疾患などの治療に不可欠です。厳格な試験により、バイオシミラーは先行バイオ医薬品の有効性と同等の効能を持つことが保証され、患者にとって不可欠な治療へのアクセスを向上させる費用対効果の高い代替手段となります。
世界市場は、手頃な価格のバイオ医薬品への需要の高まり、慢性疾患の有病率の増加、そして規制当局による承認の拡大に牽引され、急速な成長を遂げています。世界中の医療システムが高額なバイオ医薬品の経済的負担を軽減しようと努める中、バイオシミラーは現実的な解決策を提供し、腫瘍学、免疫学、眼科といった主要な治療領域における治療へのアクセスを向上させています。
リアルワールドエビデンスと堅牢な市販後調査に支えられた医師と患者の受容度向上が、バイオシミラーの採用をさらに加速させています。さらに、バイオプロセス技術と分析方法の進歩が市場の成長をさらに促進し、バイオシミラー製造の効率性と拡張性を向上させています。一方、バイオシミラーの導入を促進する政府の取り組みと、先行バイオ医薬品の特許満了が相次ぎ、新たな機会が生まれています。
市場動向
バイオ医薬品の特許満了の増加
世界的なバイオシミラーモノクローナル抗体市場の拡大は、主にブロックバスターバイオ医薬品の特許満了によって推進されており、費用対効果の高いバイオシミラー代替品への道が開かれています。ヒュミラ(アダリムマブ)、ハーセプチン(トラスツズマブ)、レミケード(インフリキシマブ)といった主要医薬品の独占権が失効したため、同等の有効性を大幅に低価格で提供するバイオシミラーの参入が可能になりました。
- 例えば、2023年1月、世界で最も売れているバイオ医薬品の一つであるアッヴィのヒュミラ(アダリムマブ)は米国における特許独占権を失い、複数のバイオシミラーの導入につながりました。これにより市場競争が激化し、大幅な価格低下が促進され、患者が手頃な価格の治療オプションにアクセスしやすくなりました。
多くの生物学的製剤が特許切れの危機に直面する中、バイオシミラーは、治療へのアクセス性を高め、手頃な価格を実現し、多様な医療現場における医療成果全体を向上させる上で重要な役割を果たすことが期待されています。
腫瘍学および自己免疫疾患における採用拡大
バイオシミラーモノクローナル抗体は、その費用対効果の高さと、先行生物学的製剤との治療的同等性から、腫瘍学および自己免疫疾患の治療においてますます採用が進んでいます。リツキシマブ、ベバシズマブ、トラスツズマブなどの主要なバイオシミラーは、リンパ腫や乳がんなどのがん治療に広く使用されています。一方、インフリキシマブとアダリムマブのバイオシミラーは、関節リウマチやクローン病などの自己免疫疾患の標準治療薬となりつつあります。
- 例えば、2024年9月にオーストラリアのがんセンターで実施された国立医学図書館の研究では、非ホジキンリンパ腫患者において、リツキシマブからバイオシミラーであるリキシミオに切り替えても、安全性、投与中止率、死亡率に有意差は認められませんでした。これらの知見は、リキシミオが安全かつ効果的な代替薬であることを裏付けており、バイオシミラーへの信頼の高まりをさらに裏付けています。
この傾向は、治療へのアクセス性を向上させ、医療費を削減し、世界的な市場の成長を促進しています。
市場概要
| 市場指標 | 詳細とデータ (2024-2033) |
|---|---|
| 2024 市場評価 | USD 14.92 Billion |
| 推定 2025 価値 | USD 17.35 Billion |
| 予測される 2033 価値 | USD 58.07 Billion |
| CAGR (2025-2033) | 16.3% |
| 支配的な地域 | 北米 |
| 最も急速に成長している地域 | アジア太平洋 |
| 主要な市場プレーヤー | Roche Holding AG, Novartis AG, Pfizer Inc., Samsung Bioepis, Amgen Inc. |
このレポートについてさらに詳しく知るには 無料サンプルをダウンロード
レポートの範囲
| レポート指標 | 詳細 |
|---|---|
| 基準年 | 2024 |
| 研究期間 | 2021-2033 |
| 予想期間 | 2026-2034 |
| 急成長市場 | アジア太平洋 |
| 最大市場 | 北米 |
| レポート範囲 | 収益予測、競合環境、成長要因、環境&ランプ、規制情勢と動向 |
| 対象地域 |
|
バイオシミラーモノクローナル抗体市場の成長要因
バイオシミラーの承認と償還政策の拡大
FDA(米国)、EMA(欧州)、PMDA(日本)などの規制当局は、バイオシミラーモノクローナル抗体の承認プロセスを合理化し、市場参入の迅速化を促進しています。同時に、政府と保険会社は、患者へのアクセス拡大とコスト削減を促進するため、償還政策を強化しています。
米国では、バイオシミラーユーザーフィー法(BsUFA)と互換性指定によってバイオシミラーの普及が促進され、欧州では入札による調達によって競争と価格の手頃さが高まっています。
- 例えば、2023年1月、米国メディケア・プログラムはインフレ抑制法に基づき、バイオシミラーに対する償還インセンティブを引き上げ、医療提供者によるバイオ医薬品の普及を促進するため、先行バイオ医薬品に対して8%の加算金を上乗せしました。
こうした取り組みにより、バイオシミラーの普及が大幅に促進され、より手頃な価格で、より幅広い患者が命を救う治療にアクセスできるようになりました。
医師と患者の受容性の向上
医療従事者におけるバイオシミラーモノクローナル抗体に対する認知度と信頼度の高まり医療提供者と患者がバイオシミラーの市場導入を牽引しています。リアルワールドエビデンス、市販後調査、そして的を絞った教育活動によって、有効性と安全性に関する懸念は効果的に解消されてきました。その結果、医師はバイオシミラーが先行バイオ医薬品と同等の治療効果を持つことを認識し、より自信を持って処方できるようになりました。一方、患者はコスト削減と必須治療へのアクセス向上という恩恵を受けています。
- 例えば、2023年にAmerican Journal of Managed Careに掲載された研究では、リウマチ専門医の80%以上が関節リウマチに対するインフリキシマブとアダリムマブのバイオシミラーの処方に抵抗がないことが明らかになりました。この広範な受け入れにより、コストの大幅な削減と生物学的療法への患者アクセスの向上が実現しました。
関係者の信頼が高まるにつれ、バイオシミラーは高価な生物学的製剤に代わる費用対効果の高い代替品として勢いを増しており、世界中で普及、価格の手頃さ、そして市場拡大を促進しています。
市場の抑制要因
高額な開発・製造コスト
バイオシミラーモノクローナル抗体の開発と製造は非常に複雑であり、高度なバイオプロセス技術、広範囲にわたる臨床試験、そして厳格な規制当局の承認が必要です。低分子ジェネリック医薬品とは異なり、バイオシミラーは、先行バイオ医薬品との構造類似性、有効性、免疫原性の同等性を証明する必要があり、研究開発、分析特性評価、医薬品安全性監視への多大な投資が必要となります。
さらに、特殊な製造施設、厳格な品質管理、そして長期にわたる開発期間がコスト高の一因となり、大幅な価格引き下げを実現することが困難になっています。比較臨床試験や市販後調査などの規制遵守要件は、費用をさらに増加させます。
これらの課題は、市場参入の遅延、競争の制限、収益性の低下を招き、小規模企業の競争を困難にし、結果としてバイオシミラーの普及を遅らせる可能性があります。
市場機会
市場拡大のためのパートナーシップとコラボレーション
バイオ医薬品企業、受託製造機関(CMO)、医療提供者間の戦略的コラボレーションは、世界的なバイオシミラーモノクローナル抗体市場の拡大において重要な役割を果たしています。これらのパートナーシップは、研究開発費の分担を促進し、規制当局の承認手続きを効率化し、流通ネットワークを強化することで、企業が財務的および技術的な障壁を克服するのに役立ちます。
さらに、グローバル企業と地域企業の合弁事業は、新興国市場への浸透を可能にします。新興国では、バイオシミラーが高価なバイオ医薬品の安価な代替品となる可能性があります。
- 例えば、2022年には、バイオコン・バイオロジクスとビアトリスが戦略的契約を締結し、トラスツズマブ、ベバシズマブ、インスリングラルギンを含むバイオシミラーポートフォリオを拡大しました。この提携により、両社は特に米国と欧州におけるグローバル市場でのプレゼンスを強化し、手頃な価格の生物学的製剤への患者アクセスを向上させました。
このような提携は、バイオシミラーの導入を加速し、生産効率を最適化し、地理的範囲を拡大することで、大きな成長機会を生み出します。
タイプ別インサイト
アダリムマブセグメントは、関節リウマチ、乾癬、クローン病などの自己免疫疾患の治療における広範な使用により、最大のシェアを占めています。ヒュミラの特許独占権の喪失により、複数のバイオシミラーの参入が可能になり、競争が激化し、治療費が低下しました。さらに、規制当局による支援、互換性の指定、そして有利な償還方針により、主要な医療市場におけるアダリムマブの採用が加速し、より広範な患者アクセスが確保され、市場の成長が促進されています。
適応症別インサイト
世界的ながん負担の高さと費用対効果の高い治療への需要の高まりにより、オンコロジーセグメントは世界市場をリードしています。ベバシズマブ、トラスツズマブ、リツキシマブのバイオシミラーは、乳がん、リンパ腫、大腸がんの治療において重要な役割を果たしています。さらに、FDA、EMA、PMDAによる規制承認の増加により、バイオシミラーの普及が促進され、有効性を維持しながら治療費を大幅に削減しています。医療制度が手頃な価格のがん治療を推進する中で、オンコロジーバイオシミラーの採用は増加し続けています。
流通チャネルに関する洞察
病院薬局は市場を支配しており、腫瘍学および自己免疫疾患治療薬の主要な流通センターとして機能しています。これらの薬局は、アクセス管理、医師の監督、保険適用を確保することで、安全で効率的な患者ケアを促進しています。さらに、政府および保険会社主導の償還制度により、病院はバイオシミラーを優先的に使用することが奨励され、より広範な採用が促進されています。病院がコスト効率の高い生物学的治療のためにバイオシミラーにますます依存するようになるにつれ、病院薬局は市場へのアクセスと手頃な価格の拡大において重要な役割を果たし続けています。
企業市場シェア
バイオシミラーモノクローナル抗体業界の主要企業は、競争優位性を獲得するために、戦略的提携、規制当局の承認取得、買収、新製品の発売といった重要なビジネス戦略の採用に注力しています。企業は研究開発への多額の投資、製造能力の拡大、そしてグローバルな流通ネットワークの強化に取り組んでいます。
Samsung Bioepis:世界のバイオシミラーモノクローナル抗体市場における新興企業
Samsung Bioepisは、腫瘍学、免疫学、眼科を専門とする大手バイオシミラー開発企業です。同社は、トラスツズマブ、ベバシズマブ、アダリムマブなど、FDAおよびEMA承認のモノクローナル抗体バイオシミラーを上市し、費用対効果の高い生物学的製剤への世界的なアクセスを向上させています。
サムスンバイオエピスの最近の動向:
- 2025年1月、サムスンバイオエピス株式会社とテバ製薬株式会社は、ソリリス(エクリズマブ)のバイオシミラーであるEPYSQLI(エクリズマブ-aagh)の米国におけるライセンス、開発、および商業化契約を締結したことを発表しました。
地域別インサイト
北米は、良好な規制環境、多額の医療費支出、そしてバイオシミラーの急速な普及に支えられ、世界のバイオシミラーモノクローナル抗体市場をリードしています。FDA(米国食品医薬品局)の生物製剤価格競争・イノベーション法(BPCIA)は承認プロセスを簡素化し、市場参入を迅速化しました。強力な償還政策、政府の優遇措置、そして保険会社の支援は、医療提供者によるバイオシミラーのより広範な導入をさらに後押ししています。
さらに、アムジェン社、ファイザー社、マイラン社といった大手企業の存在が市場の成長を後押ししています。手頃な価格のバイオ医薬品に対する需要の高まりと、医療提供者によるバイオシミラーの普及拡大が相まって、北米全域で腫瘍学、免疫学、炎症性疾患におけるバイオシミラーの普及が引き続き促進されています。
米国バイオシミラーモノクローナル抗体市場動向
米国は、多額の研究開発投資、強力な規制支援、そして革新的なバイオシミラーの発売により、市場を支配しています。FDA(米国食品医薬品局)の簡素化された承認手続きは、迅速な市場参入を促進しています。2024年5月、バイオコン・バイオロジクスはバイオシミラー「アフリベルセプト(イェサフィリ)」のFDA承認を取得し、米国眼科市場への進出を果たしました。この画期的な出来事は、バイオコンのポートフォリオ強化、価格の手頃さの向上、そして患者アクセスの向上につながります。
アジア太平洋地域は、バイオシミラー製造能力の拡大、規制当局による承認の増加、そして医療投資の増加を背景に、最も高いCAGR成長が見込まれています。中国、インド、日本、韓国などの国々は、政府の取り組み、各国のバイオ医薬品イノベーション、そしてコスト重視の医療改革に支えられ、バイオシミラー生産をリードしています。さらに、グローバル企業とアジア地域のバイオ医薬品企業間の戦略的提携により、バイオシミラーのアクセス性が向上し、この地域はバイオシミラーの開発と商業化の主要な拠点となっています。
シンガポールのバイオシミラー市場は、価値に基づく医療政策と政府の取り組みに牽引され、急速に拡大しています。例えば、2024年9月、シンガポールのケア効果庁(ACE)は価値主導型戦略を実施し、インフリキシマブ、アダリムマブ、トラスツズマブ、リツキシマブ、ベバシズマブのバイオシミラー採用率を1年以内に95%に引き上げました。この取り組みにより、80%以上の価格引き下げが実現し、5年間で1億3,600万ドルの節約が見込まれ、手頃な価格のバイオ医薬品へのアクセスが向上しました。
インドのバイオシミラーモノクローナル抗体業界は、高い疾病負担とバイオシミラー承認の増加に牽引され、急速な成長を遂げています。 2023年5月、アルケム・オンコロジーは、頭頸部がん治療薬としてセツキシマブのバイオシミラーであるセツキサを発売しました。インド医薬品管理総局(DCGI)の承認を受けたこのバイオシミラーは、エンゼン・バイオサイエンス・リミテッド社によって開発されました。この発売は、インドにおける手頃な価格、入手しやすさ、そして現地生産への注力を強化するものであり、重症患者にとってバイオシミラーへのアクセスを向上させます。
日本のバイオシミラーモノクローナル抗体市場は、有利な規制政策と商業化への取り組みの強化により成長しています。2025年1月、バイオコン・バイオロジクス社(BBL)は、日本の医薬品医療機器総合機構(PMDA)がステラーラ(ウステキヌマブ)のバイオシミラーであるウステキヌマブBS皮下注射液[YD]を承認したと発表しました。バイオコン社が開発し、株式会社陽進堂が販売するこのバイオシミラーは、手頃な価格の免疫疾患治療の選択肢を拡大し、費用対効果の高い生物学的製剤への日本の取り組みを強化するものです。
国別インサイト
- ドイツ - ドイツは、高度な医療インフラ、強力な規制当局の承認、そして新規バイオシミラーの発売により、欧州のバイオシミラーモノクローナル抗体市場において重要なプレーヤーとなっています。2024年1月、サンド社は、ポルファーマ・バイオロジクス社が開発した再発寛解型多発性硬化症(RRMS)に対する初のバイオシミラーであるTyruko(ナタリズマブ)を発売しました。この発売により、手頃な価格の多発性硬化症治療薬への患者アクセスが向上し、バイオシミラー導入におけるドイツのリーダーとしての地位が強化されます。
- 英国 - 英国のバイオシミラーモノクローナル抗体業界は、新製品の発売と手頃な価格への規制当局の支援により拡大しています。2024年3月、Dr. Reddy's LaboratoriesはベバシズマブのバイオシミラーであるVersavoを発売し、オンコロジーポートフォリオを強化しました。これは、英国のコスト抑制戦略と国民保健サービスのバイオシミラー導入イニシアチブと一致しており、より広範な患者が手頃な価格のがん治療薬にアクセスできるようにするとともに、主要なバイオシミラー企業の市場浸透を促進します。
地域別成長の洞察 無料サンプルダウンロード
バイオシミラーモノクローナル抗体市場のトップ競合他社
- Roche Holding AG
- Novartis AG
- Pfizer Inc.
- Samsung Bioepis
- Amgen Inc.
- Viatris Inc.
- Teva Pharmaceutical Industries Ltd.
- Biogen Inc.
- Celltrion, Inc.
- Fresenius Kabi AG
- Sandoz AG
- Boehringer Ingelheim International GmbH
- Merck KGaA
- Amneal Pharmaceuticals, Inc.
- Biocon Limited
最近の進展
- 2024年7月 – Amneal Pharmaceuticals, Inc.は、XOLAIRを参照するバイオシミラーであるオマリズマブをバイオシミラーパイプラインに追加することを発表しました。XOLAIRは、アレルギー性喘息および慢性特発性蕁麻疹の治療に広く使用されています。この拡大は、費用対効果の高い生物学的製剤代替品の開発に対するアムニール社のコミットメントを強化し、患者が高度なアレルギーおよび喘息治療にアクセスできるようにするものです。
アナリストの見解
当社のアナリストによると、世界のバイオシミラーモノクローナル抗体市場は、規制当局の承認増加、費用対効果の高い生物学的製剤への患者アクセス拡大、そして医療提供者による採用増加を背景に、大幅な成長が見込まれています。製造技術の重要な進歩と、バイオシミラーの有効性と安全性を裏付けるリアルワールドエビデンスが、市場浸透を加速させています。
こうした好ましい傾向にもかかわらず、世界市場はいくつかの課題に直面しています。複雑な製造プロセスと規制要件には多額の投資が必要であり、高額な開発・製造コストは依然として大きな障壁となっています。さらに、市場は、リファレンスバイオロジクスからの切り替えに依然として慎重な一部の医療提供者や患者からの抵抗に直面しています。
しかしながら、これらの課題にもかかわらず、アジア太平洋地域は特に有望な成長機会を提供しています。中国、インド、韓国などの国々では、政府がバイオシミラーの普及と医療費削減に向けた強力な取り組みを行っています。規制当局による承認プロセスの合理化と、これらの市場におけるバイオシミラーの採用拡大が進むにつれ、市場拡大に大きく貢献することが期待されます。
バイオシミラーモノクローナル抗体市場の市場区分
種類別
- アダリムマブ
- ベバシズマブ
- インフリキシマブ
- リツキシマブ
- トラスツズマブ
- その他
適応症別
- 腫瘍学
- 自己免疫疾患
- その他
流通チャネル別
- 病院薬局
- ドラッグストア・薬局
- その他
地域別
- 北アメリカ
- ヨーロッパ
- APAC
- 中東諸国とアフリカ
- LATAM
Our Clients:










































